魏珂/朱鸿明/刘中民团队合作在《Protein & Cell》发文揭示了一种心脏祖细胞的异质性及其亚群协作在心脏修复中的潜在作用
近日,魏珂教授与同济大学东方医院再生医学研究所朱鸿明研究员及刘中民教授课题组合作在Protein & Cell期刊上发表了文章“Single-cell transcriptomics of cardiac progenitors reveals functional subpopulations and their cooperative crosstalk in cardiac repair”,结合单细胞转录组学、生物信息学以及体内外实验验证,揭示了心肌球细胞内部的异质性、鉴定出功能特异性亚群并阐述了亚群间的相互作用,并通过小鼠心梗模型证实Sca-1+的CDC是促进心脏损伤修复的主要细胞类群。
心血管疾病是人类健康的主要杀手之一。随着我国经济增长和生活水平提高,心肌梗死的发病率逐年上升。尽管介入治疗、冠脉搭桥手术和药物治疗取得了长足的进步,但仍有大量心梗患者发展为心力衰竭,因此在梗死心肌的修复方面,仍亟待新技术、新策略的研究和应用。
心脏内源性的祖细胞(Cardiac Progenitors)是一群源于心肌组织、具有一定分化能力的间质细胞。尽管近年的一些谱系示踪研究发现心脏祖细胞在心肌损伤后并不能直接再生心肌细胞,但是这些祖细胞的旁分泌功能以及成血管细胞分化能力对于梗死心肌的修复依然十分重要。因此,如何提高心脏祖细胞的治疗作用依旧是心肌修复再生领域的研究热点。
心肌球来源的细胞(Cardiosphere-derived cells, CDCs)是源自心房或心室组织的间质细胞,因其可悬浮培养形成3D球状细胞团而得名。尽管实验室研究和临床试验均显示CDCs对于梗死心肌具有一定的治疗效果,但是目前CDC的分离培养依旧依赖其自身成球能力,缺乏基于细胞表面标志物的纯化环节,其内部的细胞异质性一直未见报道。解析CDCs的异质性可能揭示细胞成分和功能之间的关系,从而为阐明心脏祖细胞当前的争议提供新颖的见解。
在本文中,魏珂/朱鸿明/刘中民团队研究者通过将CDCs进行聚类分析后得到6个细胞亚群,发现:一个既往报道的干细胞标记物Sca-1(Stem cell antigen-1)的表达可将心肌球细胞区分为两个较大的亚群Sca-1+ CDCs与Sca-1- CDCs(图1:A-D)。通过将Sca-1+ CDCs、Sca-1- CDCs以及内皮细胞进行配体受体相互作用分析,发现了Sca-1+ CDCs主要作为信号的发出者,主要是促血管生成信号作用于Sca-1- CDCs(图1:E-G)。如Sca-1+ CDCs高表达的Vegfa可能以旁分泌的方式作用于Sca-1- CDCs表面受体Flt1(图1:H-I)。并进一步对两种亚群细胞的增殖、成管能力等表型进行比较,结合对特异配体和受体的干预研究,明确两亚群细胞的特性与互作方式。
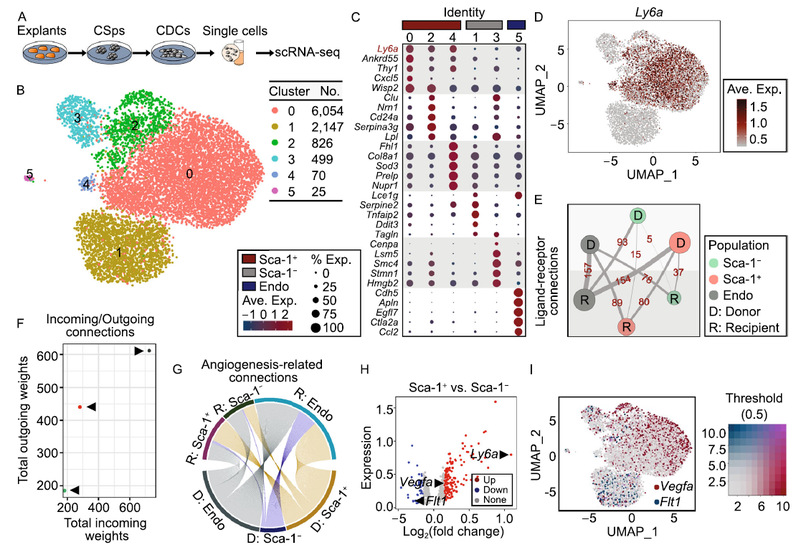
图1. scRNA-seq揭示了CDC的主要的亚群及其相互作用。
随后,研究人员分别将Sca-1- CDCs与Sca-1+ CDCs注射进梗死小鼠心肌内,以比较两种细胞在体内的治疗功能的差异。出乎意料地,仅Sca-1+ CDCs可以显著性地改善心肌梗死导致的受损心脏功能(图2:A-C)。与Sca-1- CDCs相比,在Sca-1+ CDCs中显著性上调的基因中的大多数配体均为已有报道的具有心脏保护作用的分子,例如Grem1、Cxcl12等。因此推测Sca-1+ CDCs可能通过分泌促进血管生成相关因子来促进心脏损伤修复(图2:D-E)。
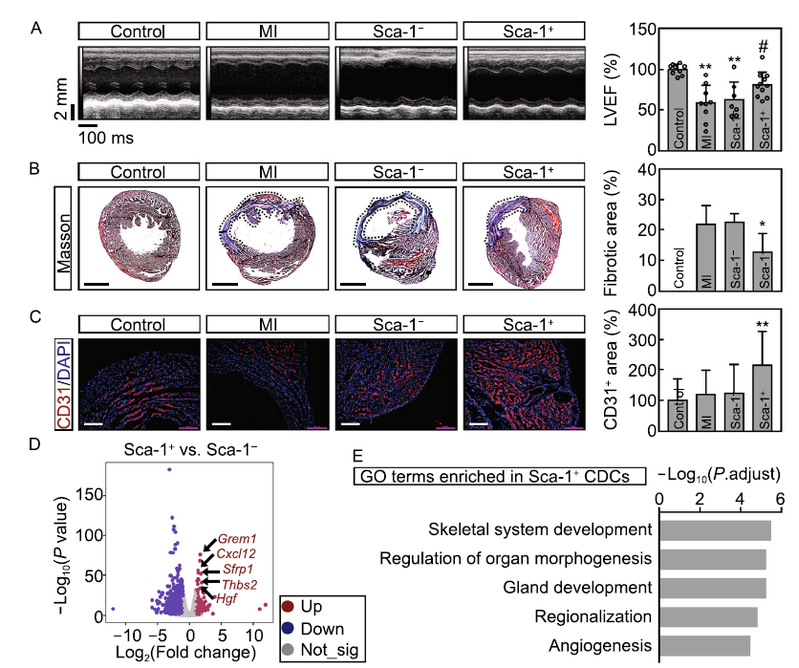
图2. Sca-1+ CDC对心肌梗死后心功能的促进作用。
综上,本研究结果揭示了一个重要的心脏祖细胞CDCs的细胞异质性,发现了功能特异性CDCs亚群及其互作机制,并证实Sca-1+的CDC是促进心脏损伤修复的主要细胞类群。本研究从细胞异质性的角度探讨影响细胞移植疗效的新因素,或有助于解释当前心脏祖细胞的争议性结果,可能对优化未来的细胞移植策略提供理论依据(图3)。
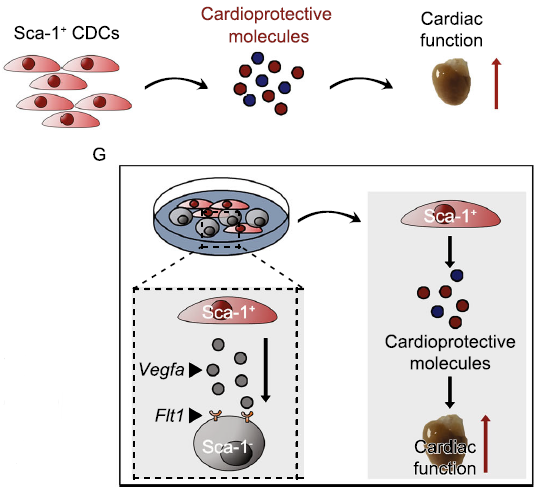
本研究的共同第一作者为同济大学医学院博士生高磊和生命科学与技术学院博士生张红杰。魏珂教授、朱鸿明研究员和刘中民教授为本文的共同通讯作者。该研究得到了科技部重点研发计划、国家自然科学基金委,上海市扬帆计划,江西省青年科学基金,同济大学中央高校基本科研业务费以及教育部细胞干性与命运编辑前沿科学中心的支持。
Copyright© 2011-2015 生命科学与技术学院, All rights reserved
地址:上海市四平路1239号 电话:021-65981041 传真:65981041


