岳锐课题组发现骨质疏松药物新靶点
2020年10月13日,国际知名杂志《Cell Reports》在线发表了同济大学生命科学与技术学院岳锐教授课题组题为“Identification of Fibroblast Activation Protein as An Osteogenic Suppressor and Anti-osteoporosis Drug Target ”的研究论文。
脊椎动物的骨骼处于动态变化中,成体骨量维持依赖于成骨细胞介导的骨生成和破骨细胞介导的骨吸收,当骨骼稳态被打破时会导致各种疾病,如骨折和骨质疏松症等。骨质疏松症(Osteoporosis)是一种以骨量减少、骨组织微结构损坏,从而导致骨脆性增加、易发生骨折为特征的全身性骨病。骨质疏松症可发生于任何年龄,但多见于绝经后女性和老年男性。研究表明,雌激素能通过抑制破骨细胞数量和功能来拮抗骨吸收,因此绝经后女性会因为雌激素水平骤减而诱发骨质疏松。大多数骨质疏松药物通过抑制骨吸收发挥作用,其中只有Romosozumab这一种药物会同时促进骨生成,但长期使用该药物会有罹患心血管疾病的风险。因此,新型骨质疏松药物的研发迫在眉睫。
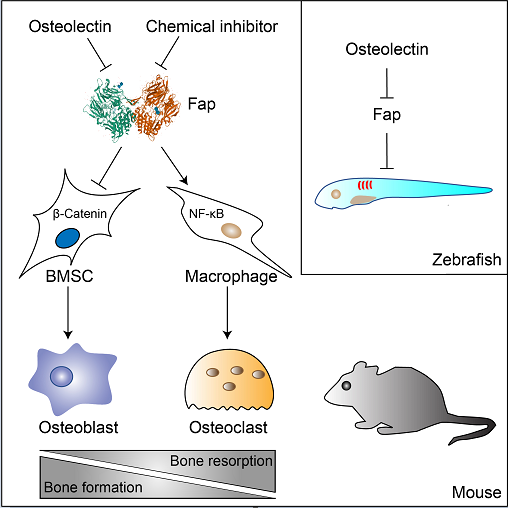
在该项研究中,研究人员通过IP-Mass spec发现新颖骨生长因子Osteolectin能够与Fap相互作用并抑制其丝氨酸蛋白酶活性。Fap基因缺失的衰老小鼠中四肢松质骨体积与野生型小鼠相比显著增加,而对野生型小鼠注射Fap抑制剂5周后可以促进骨生成、抑制骨吸收,从而显著提高长骨和脊椎松质骨体积。分子机制研究发现Fap抑制剂注射能够上调经典Wnt信号通路激活骨生成,同时下调NF-κB信号通路抑制骨吸收。细胞机制研究发现Fap抑制剂通过促进BMSC增殖进而显著促进成骨细胞分化,同时能够抑制巨噬细胞向破骨细胞分化。接下来,研究人员利用卵巢摘除小鼠构建骨质疏松模型,进一步证明了Fap抑制剂可以显著缓解骨质疏松症状,而且与骨质疏松经典药物—特立帕肽(PTH 1-34)有协同作用。最后,研究人员还在斑马鱼中发现Osteolectin可以作为Fap的内源性抑制剂促进骨矿化,从而揭示了Fap和Osteolectin具有进化上的功能保守性。该研究首次阐明了 Fap 是一类关键的成骨抑制因子,并提示Fap抑制剂有可能通过促进骨生成和抑制骨吸收的双重作用成为一类新颖的抗骨质疏松药物。
同济大学硕士生魏含静、王祎斌和博士生许艳华为本文共同第一作者。本文的其他作者还包括硕士生徐丽婷、博士生莫春阳、本科生李梁梓,以及同济大学生命科学与技术学院曹莹教授、附属口腔医院孙瑶教授、空军军医大学杨柳教授、上海交通大学医学院秦安教授和美国德克萨斯大学西南医学中心Sean Morrison教授及其团队成员。岳锐教授为本文通讯作者。本项研究获得国家重点研发计划“干细胞及转化研究”、国家自然科学基金委、中央高校基本科研业务费专项资金和教育部“细胞干性与命运编辑”前沿科学中心的大力支持。
Copyright© 2011-2015 生命科学与技术学院, All rights reserved
地址:上海市四平路1239号 电话:021-65981041 传真:65981041


